La reazione del gas tonante: esplosione di idrogeno ed ossigeno

Oltre ad un mondo piatto a cui attorno gira il sole, gli antichi immaginavano anche che DragonBall fosse finito dopo la serie GT e che l'acqua fosse un elemento unico. Le cose si sono evolute, ed ora oltre ad avere una dubbiosa nuova saga che parla di Sayan sappiamo che l'acqua è composta da idrogeno ed ossigeno.
La reazione che porta alla formazione dell'acqua viene detta esoergonica in quanto sprigiona energia (quasi come un pranzo di Natale):
"l'energia liberata per formare 200 cm³ di acqua (circa il contenuto di un bicchiere) basterebbe a scaldarne circa un litro da 25 °C fino a 100° C e a farla bollire completamente." (via: chimica.unipd.it)
Sai pensando quello che sto pensando io Billy?
Vuoi vedere quanta energia è? Benissimo.
Ma prima devi fare i compiti.
Gas tonante ed elettrolisi
Un gas formato per due parti da idrogeno ed una di ossigeno prende il nome di gas tonante, proprio per la forza dirompente con la quale avviene la reazione quando ne forniamo l'innesco: questo può essere anche solo la fiamma di una candela o una scintilla (questo è uno dei problemi dell'utilizzare l'idrogeno come carburante, il rischio di reazioni esplosive a contatto con l'aria è altissimo!).
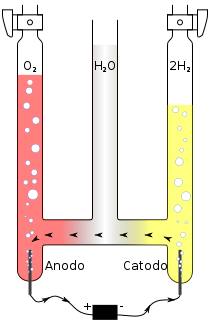
Il problema sta nel procurarsi l'idrogeno. La soluzione è l'elettrolisi (dal greco rompere con l'elettricità, ne abbiamo già parlato qui): due poli metallici vengono inseriti in acqua e viene fatta passare della corrente tramite un generatore. L'elettricità fa sì che l'elettrodo collegato al catodo assorba elettroni in un processo chiamato riduzione liberando idrogeno, mentre l'anodo li ceda in un processo chiamato ossidazione producendo ossigeno.
Le due reazioni sono quindi:
2 H+ + 2 e- → H2
4 OH- - 4 e- → 4 OH → 2 H2O + O2
Lasciando la stechiometria ai chimici, quello che interessa a noi fisici senza palestra è che il volume di idrogeno che si sviluppa è circa il doppio di quello di ossigeno: abbiamo realizzato il gas tonante.
Quello che ci resta da fare è riuscire a mettere il gas generato ad esempio in un palloncino e, con le dovute precauzioni, dare l'innesco a questa stupefacente reazione e godersi lo spettacolo.
guardate l'idrogeno tacere nel mare
guardate l'ossigeno al suo fianco dormire:
soltanto una legge che io riesco a capire
ha potuto sposarli senza farli scoppiare.

Commenti