Sapore di sale (o Quando salare l'acqua per la pasta?)

Billy hai già capito se è più conveniente coprire la pentola con il suo coperchio per far bollire prima l’acqua? Se non è così, leggi qui!
Ma cosa sai dirmi sul sale?
Dai su, non fare il timido, facciamo una sfida! Uno di noi utilizza il sale, l’altro no; mettiamo due pentole su due fornelli identici e vediamo quale delle due raggiunge per prima l’ebollizione! (Chi perde lava i piatti). Mio il gioco, mie le regole: io prendo la pentola senza sale! Mi raccomando fai in modo di abbondare con il sale.
Nota, ogni pentola contiene 2 kg (che equivale ad un volume pari a circa 2 litri) di acqua ed inoltre utilizzeremo il fornello piccolo (quello da 1000W di potenza) cosi che la nostra prova duri più tempo, che investiremo in amabile conversazione!
Come ben sai, l’acqua bolle a 100 °C (o per essere internazionali 373,16 K [kelvin]). L’ambiente in cui entrambi svolgiamo l’esperimento è lo stesso (lavoriamo nella stessa cucina: quindi medesima pressione e temperatura), per cui non iniziare a dire che sto imbrogliando!
Però io, che conosco le sacre leggi della termodinamica (più o meno) posso predire che la vincita sarà mia!
Per cui la mia acqua senza sale bollirà prima.
La mia arte divinatoria mi fa predire anche che perderai esattamente per poco più di un minuto!
No, Billy, non ho nessuna sfera di cristallo, mi sono servito solo di una banalissima calcolatrice e un minimo di conoscenza!
Ok, basta prenderti in giro; ora ti dico cosa avviene! In realtà ti ho fatto uno scherzone, o meglio, ti ho detto una mezza verità, quando, ti ho parlato del punto di ebollizione. Riformuliamo nel modo corretto: L’acqua bolle a 100 °C solo se è PURA! La tua ad esempio bollirà a circa 108 °C, proprio perché hai aggiunto un bel po’ di sale!
In cosa consiste questa stregoneria?
Billy prima di continuare definiamo un po’ di termini che saranno molto utili in seguito. Ogni qual volta ad una sostanza pura, solitamente liquida, che d’ora in poi chiameremo solvente (nel nostro caso l’acqua) si aggiunge una seconda sostanza (solida, liquida o gassosa) che prende il nome di soluto (nel nostro caso il sale); in modo tale che si disciolga e non risulti più visibile otterremo quello che in gergo tecnico si è soliti chiamare soluzione.
Ogni qual volta ad un solvente si aggiunge un soluto; quest’ultima soluzione bollirà ad una temperatura maggiore rispetto a quella del solvente puro; inoltre avrà una temperatura di solidificazione minore rispetto al caso in cui la sostanza fosse stata pura.
Billy, respira, non ti prendere di panico! I due fenomeni descritti nella definizione vengono rispettivamente chiamati innalzamento ebullioscopico ed abbassamento crioscopico.
Entrambi sono descritti dalla formula:
ΔT=K*i* m
Molto banalmente questa equazione, che rappresenta o l’aumento della temperatura di ebollizione o la diminuzione della temperatura di congelamento, è il prodotto di tre termini:
- ΔT rappresenta appunto quanti in gradi in più serviranno prima che l’acqua raggiunga l’ebollizione, o quanti gradi in meno serviranno per la solidificazione
- K è una costante. Un numero già tabulato per ogni solvente
- i è il numero di ioni in cui la molecola di solvente si dissocia una volta disciolta in acqua (o nel solvente). Solitamente, come ben sai Billy, i sali possono tendono a dividersi in due o più parti ognuna con carica positiva o negativa. Sono queste particelle cariche che si è soliti chiamare ioni! Ad esempio il comunissimo sale da cucina o cloruro di sodio (NaCl) una volta disciolto in acqua si suddividerà in Na+ e Cl-. Un altro esempio è dato dal solfito di sodio che non è altro che un conservante chimico (E221 per gli addetti ai lavori): è quello usato nei vini per aumentarne la durabilità ma inficiando incredibilmente la qualità. E’ questa fantastica sostanza che fa venire il mal di testa dopo una gran bevuta di vino scadente la sera prima. Tornando a noi, il solfito di sodio Na2SO3 si suddividerà in tre ioni. Per cui nel caso di sale al posto di i andrebbe sostituito 2, mentre se si utilizzasse come soluto il solfito di sodio bisognerebbe scrivere 3.
- Infine m è la molalità che da un’idea di quanto soluto (Billy ti ricordo che nel nostro caso è il sale) rispetto al sovente (acqua) sia stato aggiunto.
Per cui più si aggiunge del sale (nota che non è un’operazione che è possibile svolgere all’infinito poiché ad un certo punto inizierà a depositarsi sul fondo), più la temperatura di ebollizione tende ad aumentare.
Fantastico! Dopo aver fatto questa lista scientifica cerchiamo però di comprendere davvero cosa accade; altrimenti invece di perdere tempo a preparare l’occorrente per la sfida avresti potuto deliziarmi con uno squisito tiramisù!
Se fino ad ora il tutto ti è sembrato difficile ed incomprensibile, schiaffeggiati un po’, prenditi un minuto di pausa e bevi un caffè perché ora dobbiamo fare un bel passo in avanti.
Fatto? Benissimo, perché ora bisogna introdurre il concetto di potenziale chimico. Si, è una bellissima parola ed è inoltre una fantastica grandezza su cui si basa il mondo termodinamico!
Con potenziale chimico (μ) si indica la variazione di energia di un sistema (universo, quello solare, la nostra pentola con l’acqua) ogni qual volta si inserisce una sostanza esterna.
Ora Billy ascolta bene, perché quello che sto per dirti è una sacra legge che regola l’andamento del mondo: Un qualsiasi sistema tende ad evolvere verso il suo stato di minima energia! Facile da intuire se si ragiona con la logica umana. Non credo infatti Billy che tu preferiresti ad un letto, una giornata di lavoro sotto il sole! Definito questo postulato assoluto cerchiamo di capire il comportamento della nostra acqua.
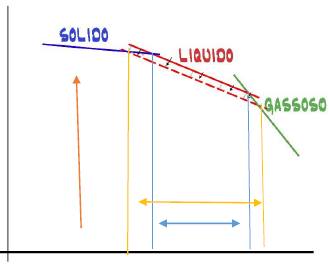
A sinistra ti ho riportato un grafico in cui sulla direzione verticale è rappresentato il nostro potenziale (approssimabile con l’energia del sistema) mentre sull’asse orizzontale è posta la temperatura in maniera crescente.
Come si interpreta?
Scelta una temperatura la si seleziona sull’asse orizzontale e tramite una retta verticale (freccia arancione) si visualizza quali dei segmenti (blu, rosso e verde) si incontra per primo, per cui quale stato a quella temperatura abbia energia minore. Individuando così la forma in cui si trova la sostanza. Nel caso rappresentato si vede che si è considerata una temperatura relativamente bassa per cui lo stato in cui sarà l’acqua è quello solido.
In questo grafico inoltre possono essere estrapolate altre due informazioni:
- La mia incapacità di disegnare linee dritte
- Quello che succede all’acqua una volta che si è aggiunto del sale
Mentre il primo punto è evidente, Billy, e non ha bisogno di ulteriori spiegazioni approfondiamo il secondo. Nello stato puro l’acqua, quando è liquida, possiede un determinato potenziale chimico che determina un intervallo di temperatura (doppia freccia azzurra) in cui è possibile visualizzare l’acqua in questo stato. Quando si aggiunge del sale invece avviene che l’energia dello stato liquido si abbassa, (linea rossa tratteggiata); andando ad intersecare prima la linea del solido e dopo quella del gas: costituendo così un intervallo maggiore di temperature (doppia freccia gialla) rispetto al caso precedente in cui l’acqua sarà stabile liquida.
Per cui dopo l‘aggiunta di sale l’acqua solidificherà a temperature più basse (abbassamento crioscopico) mentre bollirà a temperature maggiori (innalzamento ebullioscopico).
So che la tua immensa curiosità Billy spinge a chiederti perché l’energia del sistema liquido tenda ad abbassarsi dopo l’aggiunta del sale ed io, che non voglio lasciarti andare via con dei dubbi, rispondo subito!
Ahimè, però dobbiamo introdurre un altro concetto termodinamico: l’entropia! Turbamenti e dolori per ogni studente! In prima approssimazione possiamo definire l’entropia come lo stato di disordine di un sistema. Ora apri bene le orecchie. Ogni sistema, oltre ad adorare il suo stato di minima energia, preferisce mantenere il più possibile uno stato disordinato proprio perché abbassa ancora di più il suo stato energetico!
Anche in questo caso ragioniamo con la logica umana! Billy dopo una serata in cui ti sei dato ai bagordi, dove hai bevuto un sacco di vino di ottima qualità (est! est!! est!!!) privo di E221, torni a casa. Nonostante i fumi dell’alcol abbiano annebbiato la tua coscienza, sai che coricarsi con i vestiti non è il massimo. Per cui ti spogli rapidamente e lanci disordinatamente i vestiti sulla sedia, posta in camera tua proprio per svolgere il ruolo di armadio secondario. Come puoi ben intuire, hai preferito lanciare i vestiti alla rinfusa piuttosto che raccoglierli ordinatamente, proprio perché la prima azione ti ha fatto raggiungere il caro amico Morfeo! E non devo essere io a dirti che il letto è il tuo stato energetico più basso in questa situazione, Billy!
Per cui quando un qualsiasi sistema ne avrà la possibilità preferirà rimanere in uno stato disordinato, così da possedere minore energia. Billy quando all’acqua aggiungi del sale, abbassi la sua energia, proprio perché fornendo un numero maggiore di particelle le consenti di creare maggiore disordine!
Credo che ormai tu abbia finalmente capito, Billy, perché aggiungere il sale alza la temperatura di ebollizione. Un altro arcano della scienza ti è stato svelato. Continua ad amare il metodo sperimentale e ad incuriosirti per le piccole cose poiché “Accidere ex una scintilla incendia passim”.

Commenti